УДК 619:615.31:615.012.1577.0
ПРОТИВОПАРАЗИТАРНАЯ АКТИВНОСТЬ ФАМЕКТИНА И СОЕДИНЕНИЙ РАЗЛИЧНОЙ ХИМИЧЕСКОЙ ПРИРОДЫ
М.Х. ДЖАФАРОВ, М.Н. МИРЗАЕВ, И.В. ЗАВАРЗИН
Исследовали противопаразитарную активность серии полученных полусинтетических производных 16-членных макролидов (фамектина), некоторых соединений стероидной природы и трансформированного пролина с применением олигохет Tubificidal tubifex в качестве тест-объектов. У ряда изученных соединений обнаружено эффективное противопаразитарное действие.
Ключевые слова: противопаразитарная активность, полусинтетические 16-членные макролиды, адермектин, фамектин, стероиды, трансформированный пролин, олигохета.
Как известно, авермектинсодержащие препараты обладают широким спектром инсектицидного, акарицидного и нематоцидного действия в относительно низких дозах, поэтому отпадает необходимость многократной обработки животных при смешанных инвазиях. Однако данные некоторых исследователей свидетельствуют о селекции устойчивых форм возбудителей и снижении эффективности многих известных противопаразитарных препаратов указанной группы (1, 2), в связи с чем поиск перспективных противопаразитарных средств широкого спектра действия представляет большой теоретический и практический интерес. По нашему мнению, к таким соединениям могут быть отнесены макролиды (1, 2) и стероиды (3), а также цис-5-фенилпролин (4).
Часто модификация известных противопаразитарных и антибактериальных средств определенной химической природы (производные бензимидазола, макролиды, пенициллины, глюкозамины, никотиноиды) (5) принципиально не меняет молекулярных механизмов их действия, однако позволяет относительно быстро реагировать на развитие резистентности и преодолевать ее на некоторый (обычно относительно короткий) период. Стероиды привлекательны тем, что они как эндогенные липофильные метаболиты могут использоваться в качестве платформы — молекулярного переносчика какого-либо биологически активного противобактериального или противопаразитарного структурного фрагмента за счет его ковалентного связывания с молекулой стероида и целевой доставки в органы и клетки-мишени. Такой переносчик может перемещать действующее вещество как на межклеточном уровне, так и внутри клетки от ее цитоплазматической мембраны до ДНК. В частности, сообщалось, что гликозид ситостерина — β-ситостерол-3-О-глюкопиранозид может рассматриваться в качестве одного из перспективных ингибиторов открытой недавно бактериальной сортазы (6). Стероидные соединения также привлекательны как антиинфекционные средства в связи с обнаружением у некоторых патогенных микроорганизмов (возбудители туберкулеза, чумы, тифа, сибирской язвы, холеры и др.) немевалонатного пути биосинтеза важного метаболита при образовании изопреноидов — изопентенилпирофосфата (7). В этой связи интересно вспомнить знаменитую фузидиевую кислоту — изопреноид с 19-ретроструктурой (оказывает бактериостатическое действие на стафилококки, менингококки, гонококки) (8).
Для решения поставленной задачи нами была создана серия соединений различной химической природы (способы получения соединений и препараты на их основе будут защищены патентами). Ранее мы обнаружили, что некоторые полусинтетические производные 16-членных макролидов обладают эффективным противопаразитарным действием, и впервые сообщили о выявлении такой активности у ряда соединений стероидной природы (9, 10).
Цель настоящей работы заключалась в изучении противопаразитарного эффекта фамектина, а также органических соединений стероидной и иной химической природы.
Методика. Сравнивали действие известных (абамектин, клозантел) и предлагаемых органических соединений с рабочими названиями Ad (адермектин) (10), Fab (фамектин), R-407, R-408, R-412, R-413, Ch-243, KUD-735 (4), а также композиции Ad с pro-S-1.1 (10) в разных соотношениях (1:10, 1:100). В качестве тест-объектов при экспресс-оценке биоцидной активности использовались олигохеты Tubificidaltubifex (11). Острую токсичность препарата Fab определяли, как описано (12), на стандартных лабораторных белых мышах с живой массой 19-20 г при введении внутрибрюшинно (животные использовались с учетом требований Европейской конвенции по защите позвоночных животных, применяемых для экспериментальных и других научных целей) (86/609 EEC).
Результаты. Аd и Fab имеют макролидную природу (получены химической модификацией 16-членных макролидов — авермектинов, продуцируемых почвенным микроорганизмом Streptomycesavermitilis) (13). Соединения с символами R-407, R-408 и т.д., Ch-243 и pro-S-1.1 представляют собой вещества стероидной природы (3, 9), содержащие активные функциональные группы в положениях С-3 и С-20 или С-6, KUD-735 — трансформированный пролин с потенциальным центром ингибирования изоформы SrtA сортазы Staphylococсusaureus (4) (рис.).
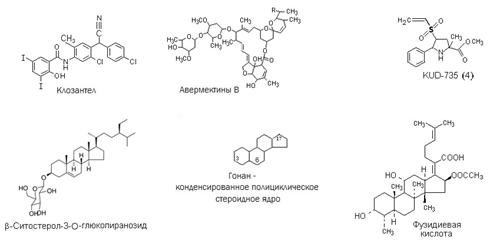 |
Химическая структура некоторых соединений, обладающих противопаразитарной активностью. R — метильная или этильная группа. |
Исследования противопаразитарной активности выбранных соединений показали, что абамектин парализует 50 % олигохет при концентрации 5,0 мкг/мл через 30 мин действия. Аналогичный эффект мы наблюдали у клозантела при концентрации 10 мкг/мл через 180 мин, у соединений Ad и Fab при концентрации 5,0 мкг/мл через 30 мин, а у композиций Ad с pro-S-1.1 (1:10 и 1:100) — при концентрациях соответственно 10 и 5 мкг/мл (табл.).
При оценке острой токсичности было установлено, что ЛД50 для белых мышей у препарата Ad составляет 35,96 мг/кг, ЛД100 — 69,44 мг/кг. ЛД50 и ЛД100 препарата Fab равнялись соответственно 36,45 и 72,31 мг/кг. Эти показатели сопоставимы со значениями ЛД50 для применяемых в настоящее время авермектиновых препаратов: для абамектина — 19, ивермектина — 53 и аверсектина С — 90 мг/кг (14).
| Сравнение биоцидного действия изученных соединений разной химической природы (макролиды, стерины и трансформированный пролин) в экспресс-тесте на олигохетах Tubificidaltubifex | ||||
Исследуемое вещество |
Концентрация, мкг/мл |
Время действия, мин |
||
30 |
60 |
180 |
||
Абамектин (Аб) |
5,0 |
++ |
+++ |
+++ |
Адермектин (Ad) |
5,0 |
++ |
++ |
+++ |
Клозантел |
5,0 |
0 |
+ |
+ |
Fab (фамектин) |
5,0 |
++ |
++ |
+++ |
R-407 |
5,0 |
0 |
0 |
0 |
R-408 |
5,0 |
0 |
0 |
0 |
R-412 |
5,0 |
0 |
0 |
0 |
R-413 |
5,0 |
0 |
0 |
0 |
Ch-243 |
5,0 |
0 |
+ |
+ |
KUD-735 |
5,0 |
0 |
+ |
+ |
Композиция Ad с pro-S-1.1: |
|
|
|
|
1:10 |
5,0 |
+ |
++ |
+++ |
1:100 |
5,0 |
++ |
++ |
+++ |
П р и м е ч а н и е. Описание соединений см. в разделе «Методика». 0 — нет действия; «+», «++», «+++» и «++++» — паралич соответственно менее 50 %, 50-60 %, 60-80 % и 80-100 % особей. |
||||
Клиническая картина интоксикации у мышей была сходной (мышечная дрожь, судороги). У всех наблюдалось нарушение координации движений, затем наступало сильное угнетение, животные лежали, у них отсутствовали реакции на внешние раздражители. Через 20-30 мин происходила гибель мышей. При вскрытии как павших, так и убитых по окончании эксперимента особей видимых патологических изменений не отмечали.
Таким образом, испытанные вещества по степени воздействия на организм согласно нормативами ГОСТ 12.1.007-76 относятся ко II классу опасности (вещества высокоопасные).
Для исследованных соединений характерно наличие структурного фрагмента, содержащего кето- или полярную функциональную группу (–ОН, –SH, =NH, =O, =S и др.). Анализ на моделях Дрейдинга показывает, что в этих соединениях функциональные группы могут располагаться под углом около 90° относительно средней плоскости циклической структуры макролидного или стероидного ядра, и такая конфигурация, по-видимому, способствует взаимодействию с рецепторами в мишенях.
На основе Ad и Fab были разработаны экспериментальные формы коммерческих противопаразитарных средств, которые, по предварительным данным, достаточно эффективны. У средства на основе Ad также подтверждена высокая стабильность: при хранении в течение 1 года противопаразитарная активность не утрачивалась (результаты исследований по фармакодинамике и фармакокинетике разработанных препаративных форм на основе Ad и Fab будут опубликованы в отдельном сообщении).
Итак, из изученной серии соединений разной химической природы (макролиды, стероиды, трансформированный пролин, композиция макролидов со стероидами) адермектин (Ad), фамектин (Fab), Ch-243, а также композиции на основе Ad и pro-S-1.1 (с разным соотношением компонентов) обладают эффективным противопаразитарным действием и могут быть перспективными при создании биоцидных препаратов для применения в животноводстве.
Л И Т Е Р А Т У Р А
1. С т р а ч у н с к и й Л.С., К о з л о в С.Н. Макролиды в современной клинической практике. Смоленск, 1998.
2. Macrolide antibiotics. Chemistry, biology and practice /S. Omura (ed.). N.Y., Elsevier Science, 2002.
3. Д ж а ф а р о в М.Х., З а й ц е в С.Ю., М а к с и м о в В.И. Стероиды. Строение, получение, свойства и биологическое значение. Применение в медицине и ветеринарии. СПб, 2010.
4. K u d r y a v t s e v K.K., B e n t l e y M.L., M c C a f f e r t y D.G. Probing of cis-5-phenyl proline scaffold as a platform for the synthesis of mechanism-based inhibitors of the Staphylococus aureus sortase SrtA isoform. Bioorg. Med. Chem., 2009, 17: 2886-2893.
5. Л о п а т и н а Ю.В., Е р е м и н а О.Ю. Применение инсектицидов группы неоникотиноидов в ветеринарии. С.-х. биол., 2005, 6: 14-24.
6. S u r e e N., Y i S.W., T h i e u W., M a r o h n M., D a m o i s e a u x R., C h a n A., J u n g M.E., C l u b b R.T. Discovery and structure-activity relationship analysis of Staphylococcus aureus sortase A inhibitors. Bioorg. Med. Chem., 2009, 17: 7174-7185.
7. R o h d i c h F., B a c h e r A., E i s e n r e i c h W. Isoprenoid biosynthetic pathways as anti-infective drug targets. Biochem. Soc. Trans., 2005, 33: 785-791.
8. М а ш к о в с к и й М.Д. Лекарственные средства. М., 2010.
9. Д ж а ф а р о в М.Х., З а й ц е в С.Ю., М и р з а е в М.Н. и др. Синтез и биологическая активность стероидных дигидропиразолов. Российский иммунологический журнал, 2008, 2(11)/2-3: 192.
10. D z h a f a r o v M.Kh., Z a i t s e v S.Yu., M i r z a e v M.N., U r a z a e v D.N., M a x i m o v V.I. Antiparasitic activity of adermectin and compounds of a steroid nature. Russ. Agr. Sciences, 2010, 36(2): 130-132.
11. Д р и н я е в В.А., Ч и ж о в В.Н., К о в а л е в В.Н., М и р з а е в М.Н. Способ определения нематоцидной активности авермектинов. Патент РФ ¹ RU 2013053 C1; A01N63/00, опубл. 1994.
12. Х а б р и е в Р.У., Д е н и с о в И.Н., Г е р а с и м о в В.Б., К у к е с В.Г. и др. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. М., 2005.
13. I k e d a H., O m u r a S. Avermectin biosynthesis. Chem. Rev., 1997, 97(7): 2591-2610.
14. Г у л ь ч и н с к а я Т.С. Авермектинсодержащие инъекционные лекарственные средства на российском рынке ветпрепаратов. http://www.vettorg.ru/magazines/?magid=2&year= 2001&issid=9&artid=91.
ANTIPARASITIC ACTIVITY OF FAMECTIN AND SOME COMPOUNDS OF DIFFERENT CHEMICAL NATURE
M.Kh. Dzhafarov, M.N. Myrzaev, I.V. Zavarsin
Semisynthetic derivatives of avermectins, famectin, and some compounds of steroidal and other chemical nature were tested as biocide agents. The antiparasitic activity was determined with application of oilgohets Tubificidal tubifex as test-objects. Some of these compounds demonstrate the effective antiparasitic action.
Keywords: antiparasytic activity, semisynthetic 16-membered macrolides, adermectin, famectin, steroids, transformed proline, oligochaeta.
ФГОУ ВПО Московская государственная |
Поступила в редакцию |













